|
Hệ thống phân cấp MedDRA “MedDRA Hierarchy”
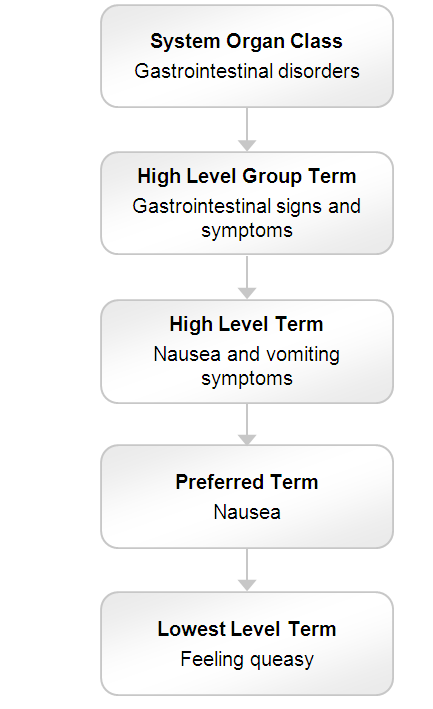
Cấu trúc của MedDRA rất logic. Có năm cấp độ trong hệ thống phân cấp MedDRA, được sắp xếp từ rất cụ thể đến rất chung chung. Ở cấp độ cụ thể nhất, được gọi là “Điều khoản cấp thấp nhất” (LLT - Lowest Level Terms), có hơn 80.000 điều khoản tương ứng với cách thông tin được truyền đạt. Những LLT này phản ánh cách một quan sát có thể được báo cáo trong thực tế. Cấp độ này hỗ trợ trực tiếp việc chỉ định các thuật ngữ MedDRA trong cơ sở dữ liệu người dùng.
Mỗi thành viên của cấp độ tiếp theo, "Thuật ngữ ưu tiên" (PTs - Preferred Terms), là một mô tả riêng biệt (khái niệm y tế duy nhất) cho một triệu chứng, dấu hiệu, chẩn đoán bệnh, chỉ định điều trị, điều tra, thủ thuật phẫu thuật hoặc y tế và đặc điểm lịch sử y tế xã hội hoặc gia đình . Mỗi LLT chỉ được liên kết với một PT. Mỗi PT có ít nhất một LLT (chính nó) cũng như các từ đồng nghĩa và biến thể từ vựng (ví dụ: viết tắt, thứ tự từ khác nhau).
Các PT liên quan được nhóm lại với nhau thành “Các thuật ngữ cấp cao” (HLT - High Level Terms) dựa trên giải phẫu, bệnh lý, sinh lý học, nguyên nhân hoặc chức năng. Các HLT, có liên quan với nhau về mặt giải phẫu, bệnh lý, sinh lý học, căn nguyên hoặc chức năng, lần lượt được liên kết với “Các thuật ngữ nhóm cấp cao” (HLGTs - High Level Group Terms).
Cuối cùng, HLGT được nhóm thành “Các loại cơ quan hệ thống” (SOC - System Organ Classes) được nhóm theo nguyên nhân (ví dụ: Nhiễm trùng “Infections” và nhiễm ký sinh trùng “infestations”), vị trí biểu hiện (ví dụ: Rối loạn tiêu hóa “Gastrointestinal disorders”) hoặc mục đích (ví dụ: Thủ tục phẫu thuật và y tế). Ngoài ra, có một SOC để chứa các vấn đề liên quan đến sản phẩm và một để chứa các hoàn cảnh xã hội.
|
|